22.03.2023 в лаборатории биологии и химии центра «Точка роста», на уроке химии, с обучающимися 9 класса ГБОУ ООШ с. Каменка были проведены эксперименты с использованием цифровой лаборатории на темы: «Растворение – физико-химический процесс», «рН среда в солях».
Что же происходит при растворении вещества?
Во-первых, при растворении вещество дробится до молекул, которые равномерно распределяются среди молекул растворителя, смешиваются с ними – это физическая сторона процесса растворения.
Во-вторых, происходит взаимодействие растворенного вещества с молекулами растворителя. Образующиеся при этом соединения непрочные и имеют переменный состав в зависимости от температуры, содержания вещества и других факторов. Образование этих соединений, т.е. химический процесс, сопровождаемый растворение, характеризуется теми же признаками, по которым мы определяем химические реакции: выделение или поглощение теплоты, изменения окраски и т.д.
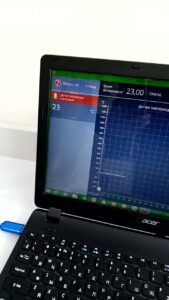
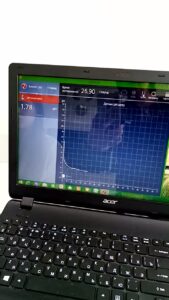
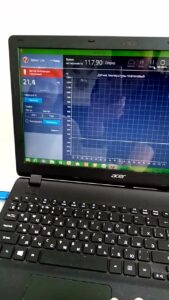
Используя датчик температуры проверили экспериментально, действительно растворение – химический процесс. Растворяли в воде кислоту, аммиачную селитру. В первом случае по датчику зафиксировали повышение температуры, а во втором – понижение.
Следующий эксперимент касался растворов солей. Рассмотрели гидролиз солей – взаимодействие ионов, входящих в состав соли с водой. Перед обучающимися стояла задача в определении рН среды солей. рН -среда — водородный показатель кислотности среды, характеризующийся наличием ионов водорода (Н+). Если ионов водорода в среде много, она кислая, если мало — щелочная.
В химии существует следующее правило:
Если соль образована сильным основанием и слабой кислотой, то реакция среды щелочная. С использование датчика рН -метра проверили соль карбоната натрия. рН среда определилась в цифровом значении выше восьми, что свидетельствует о щелочной среде. Далее, соль хлорида меди, образованная слабым основанием и сильной кислотой, рН среда оказалась ниже 5, что говорит о кислой среде. Соли хлорида натрия, образованная сильным основанием и сильной кислотой, карбоната алюминия, образованная слабым основанием и слабой кислотой, показали нейтральную среду. Цифровые показания подтвердили и индикаторы. В эксперименте был использован универсальный индикатор.
Область применения водородного показателя очень широка: это химия, пищевая промышленность, экология, биология, медицина. Утоляя жажду, мы пьем воду и различные напитки, но как это отразится на кислотно-щелочном баланс внутренней среды организма, ведь биохимические процессы должны протекать при строго заданной кислотности. Нарушение правил питания может повлиять на здоровье в целом, спровоцировав появление щелочной или среды с повышенной кислотностью в организме. Следствие этого: нарушение в деятельности желудочно-кишечного тракта и дыхательных путей.
При исследовании почвы рН является одной из наиболее важных характеристик. По значению рН, в частности, можно судить о содержании в почве питательных веществ, а также о том, какие растения могут успешно расти на данной почве. Например, рост фасоли, салата, черной смородины затрудняется при рН почвы ниже 6,0; капусты – ниже 5,4; яблони – ниже 5,0; картофеля – ниже 4,9. Кислые почвы обычно менее богаты питательными веществами, необходимыми растениям.
Косметические и моющие средства должны иметь оптимальное значение рН для того, чтобы при их применении не страдала кожа, поэтому их необходимо проверять перед использованием. Например: Косметические средства с рН от 5,5-7 универсальны и их могут использовать люди с различными типами кожи, не нанося ущерба своему организму, для сухой кожи подходят косметические средства с рН от 3-4 до 5,5, для жирной кожи подходят косметические средства с рН от 7 до 9.
Учитель завершила урок следующими словами: на внеурочных занятиях проведем исследование различных напитков, моющих и косметических средств и составим каталог о величине их рН с выводом о влиянии данного продукта на здоровье человека.